肠道菌群竟然还会影响近视!Cell Discovery:Akkermansia菌代谢产物3-IAA有望阻止高度近视进展
时间:2024-10-20 15:02:08 热度:37.1℃ 作者:网络
在这个数字时代,眼睛几乎成了最忙碌的“器官”,长时间盯着屏幕,不仅让视力悄悄下滑,还可能引发各种眼部不适。为了防治近视,大家都说要保护用眼,对此,富含叶黄素的食物吃吃吃,眼保健操、贴眼贴等护眼方法接踵而来,可是,谁知道肚子里肠菌竟然也参和了进来!
复旦大学附属眼耳鼻喉科医院竺向佳、卢奕等人在Cell Discovery期刊上发表了研究成果。通过对高度近视(HM)患者的肠道微生物和代谢物进行深入分析,发现益生菌Akkermansia的定植以及肠菌代谢物吲哚-3-乙酸(3-IAA)的水平与近视的发展程度紧密相关。研究提出了肠道和眼睛之间的相互作用,即肠道-眼轴,以及肠道微生物群在HM发病机制中的潜在作用。

研究内容与思路
一、高度近视的严重程度与肠道菌群失调有关
作者对患者粪便样本进行了测序,发现HM组和正常组的肠道微生物群的丰富度和多样性存在差异:在HM组中,Akkermansia、Fusobacteriaceae、Tissierellaceae、Parvimonas、TM7-3、Gemella和 Carnobacteriaceae表达显著减少,而 Pasteurellaceae、Gemmatimonadetes、Butyricicoccus 和 Lautropia 富集;其中,Akkermansia是一种对各种疾病有影响的益生菌,与HM相关性最强。
使用双样本孟德尔随机化(MR)分析进一步探索HM与肠道菌群之间的因果关系,发现14种细菌与HM具有显著因果关系。其中g Akkermansia成为HM的保护因素。进一步分析了菌群与评估HM严重程度的两个参数(AL 和屈光不正)之间的相关性,发现 Akkermansia 与 AL 呈负相关。
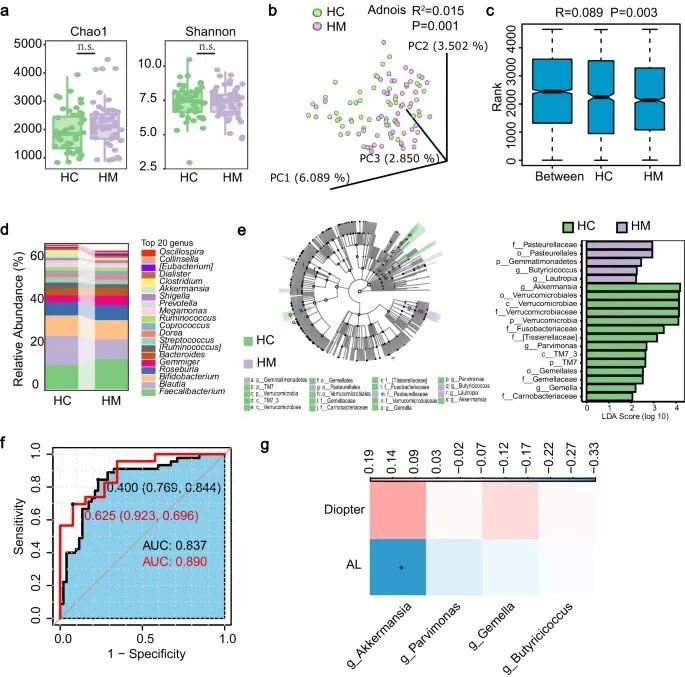
研究思路:作者首先进行测序探讨HM与肠道菌群的联系,发现HM患者肠道菌群的组成与健康人群存在显著差异,特别是益生菌Akkermansia的减少与HM的严重程度密切相关。这表明肠道菌群的失衡可能在HM的发展中起到了促进作用。
二、健康的肠道菌群可维持巩膜中COL1A1表达,从而延缓HM
作者给与小鼠抗生素混合物(ABX)治疗以清除小鼠自身肠道菌群,之后将两组参与者的粪便定植到小鼠中。测序发现细菌在受体小鼠中成功定植。对移植了正常人群菌群的小鼠(FMTHC)、HM人群菌群的小鼠(FMTHM)、ABX小鼠和正常小鼠进行近视诱导,发现所有小鼠均表现出显着的近视变化和AL伸长,但FMTHC小鼠的近视进展显著慢于FMTHM,这表明健康的肠道菌群可以延缓近视进展。
COL1A1是巩膜细胞外基质(ECM)的主要成分,在近视进展中表达被抑制,而FMTHC治疗显著抑制了HM诱导的COL1A1减少。
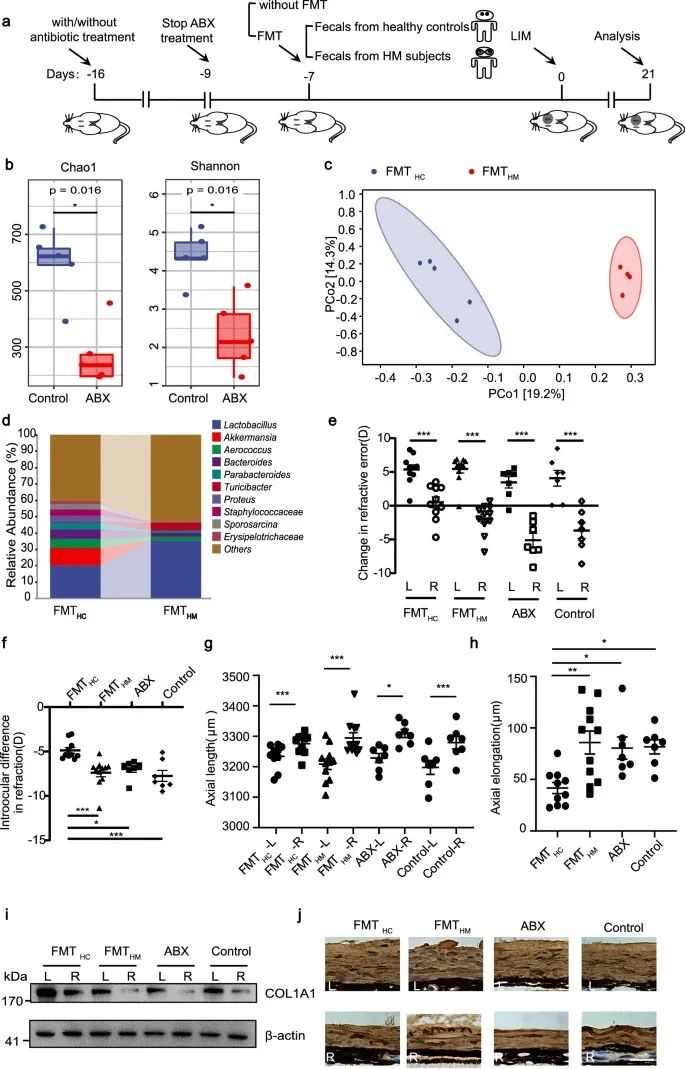
研究思路:发现肠道菌群对HM存在影响后,作者开展了动物实验,通过菌群定植来直观明确HM是否受到菌群的影响。肯定了菌群对HM起重要作用后,作者还检测了巩膜ECM主要成分是否与此有关。
三、肠道菌群失调导致血浆3-IAA水平降低
作者进行了有针对性的定量代谢组学分析,以进一步探索可能与肠道菌群失调相关的血浆代谢组变化。共鉴定出193种代谢物,相对丰度分析发现HM组内吲哚水平的显着降低,进一步发现HM组中存在2 种上调的代谢物和 5 种下调的代谢物,其中,3-IAA 显示出最明显的下降。
代谢物与HM严重程度之间的相关性分析显示,HM和HC受试者血浆吲哚-3-丙酸、己二酸和3-IAA 水平与AL呈负相关。此外,Akkermansia丰度与3-IAA水平呈正相关。
作者检测了FMTHC和FMTHM小鼠血浆3-IAA浓度,发现FMTHC小鼠的血浆 3-IAA浓度更高。以上结果表明来自HC受试者的完整肠道微生物群具有更强的产生3-IAA的能力,这强调了3-IAA在HM进展中的重要性。
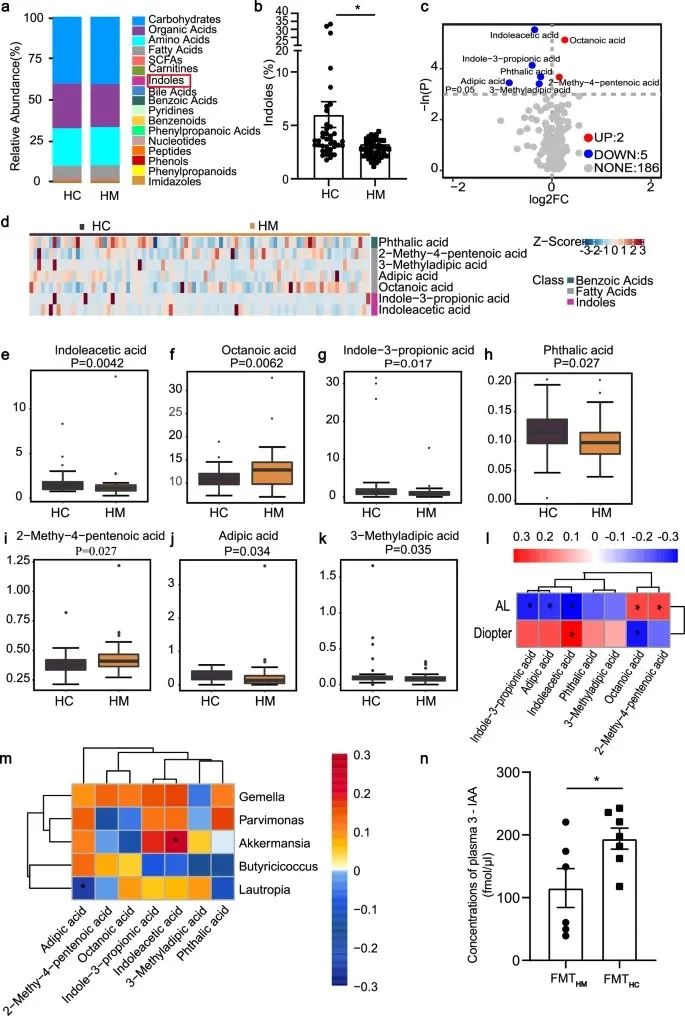
研究思路:那么,涉及到肠道菌群,则常常与代谢密切相关,对此,作者进行了代谢组学分析以便挖掘相关代谢产物,发现3-IAA,动物实验发现3-IAA在FMTHM小鼠这表达被抑制,而FMTHC小鼠中表达增加,肯定了3-IAA在这一环节的作用,暗示3-IAA可能在抑制HM进展中发挥了保护作用。
四、每日补充3-IAA可通过提高巩膜中COL1A1的表达来缓解HM的进展
作者在近视诱导前7天开始给与小鼠3-IAA,发现相比于空白组,近视诱导组和3-IAA+近视诱导组在散焦眼中均表现出显着的近视变化和AL伸长。但3-IAA组近视屈光不正显著减少,AL伸长率减少,且COL1A1表达增加。这些发现表明3-IAA有可能缓解HM的进展。
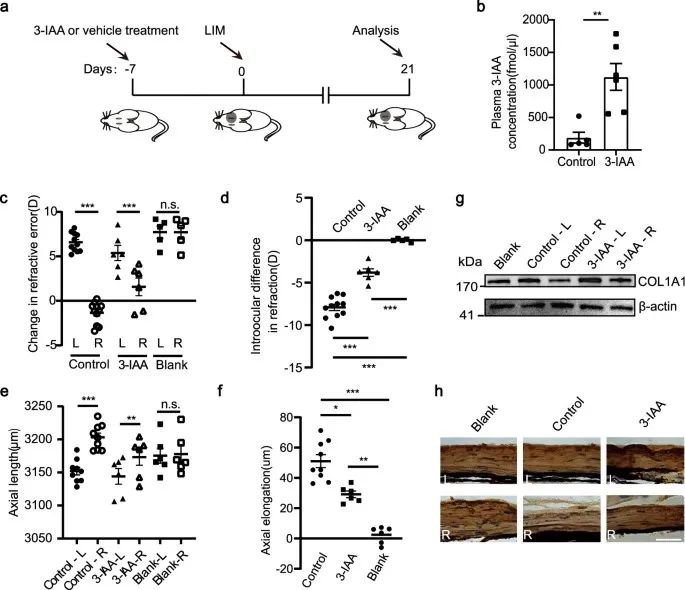
研究思路:检测到3-IAA在HM过程中发挥作用后,作者开展了动物实验,外源性给予3-IAA来明确3-IAA是否真的可以延缓HM进展。
五、3-IAA 在体外促进 COL1A1 的表达,独立于芳烃受体 (AHR) 通路
作者开展了体外实验来探讨3-IAA对COL1A1表达的影响,发现经过3-IAA治疗后,COL1A1表达增加。鉴于3-IAA已被报道为AHR的内源性配体,作者探讨研究了3-IAA是否通过AHR通路促进COL1A1表达。实验发现3-IAA显着增加了AHR的已知靶基因CYP1A1的mRNA表达水平,但敲低AHR后,3-IAA对COL1A1表达的刺激作用并未消除。这些发现表明,3-IAA对COL1A1的促进作用与AHR通路无关。
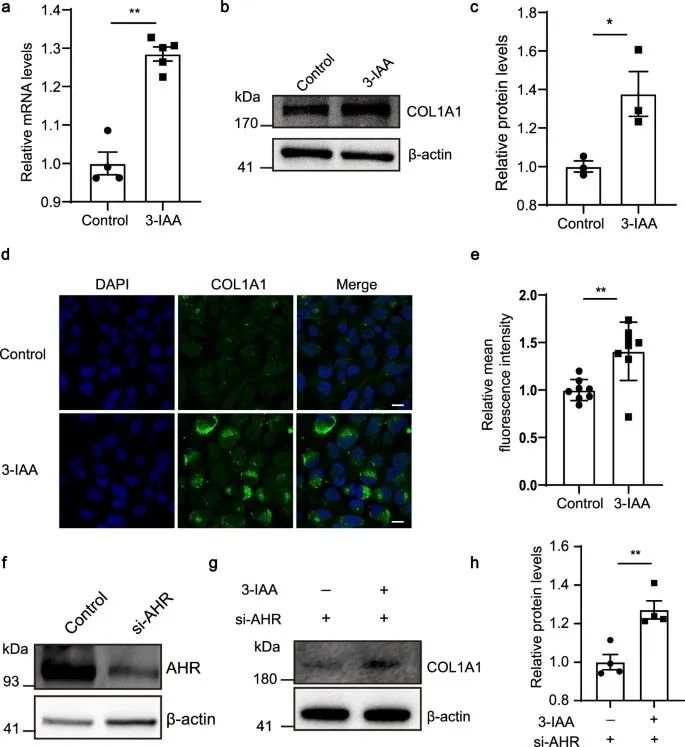
研究思路:明确了3-IAA影响HM后,进一步则是探讨其作用机制。作者从已有研究入手,探讨3-IAA是否通过已被证实的AHR通路来发挥调节HM作用。
六、3-IAA通过增加其启动子中 SP1 的富集来转录激活 COL1A1 表达
为了研究3-IAA如何调节COL1A1表达,作者检测了参与COL1A1调节的关键调节因子表达水平。研究发现-IAA显着增加了胶原蛋白调节和近视发展的关键转录因子SP1的表达。敲低SP1后,3-IAA对COL1A1的刺激作用被消除。
对此,作者体外实验研究了3-IAA如何通过SP1调节COL1A1表达。通过数据库分析发现两个SP1经典结合位点与COL1A1最为相关,CUT&Tag 测定发现SP1与COL1A1启动子区域的结合显著增加。进一步实验发现3-IAA 可显著上调COL1A1启动子活性。
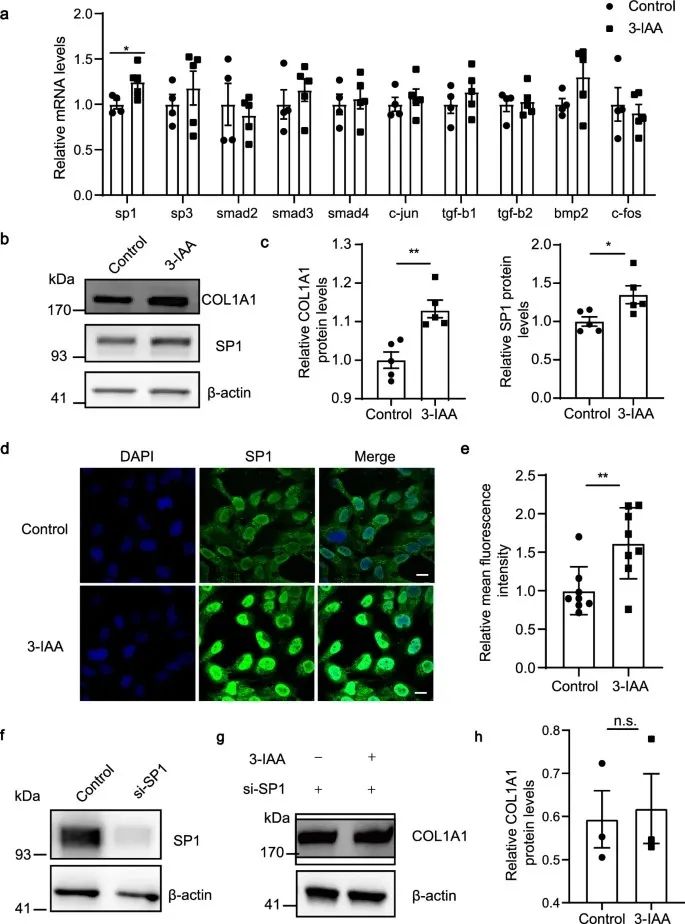
研究思路:3-IAA不是通过AHR通路发挥作用,表明3-IAA可能通过其他信号通路来调节COL1A1的表达。作者从参与COL1A1调节的关键调节因子入手,结合数据库分析以及实验验证,发现3-IAA通过增加转录因子SP1在COL1A1基因启动子区域的富集,促进了COL1A1的转录激活。
小结
综上所述,这项研究通过测序分析、肠菌定植、外源性补充代谢产物等实验方式证实了HM受肠道菌群及其代谢产物的影响,尤其是Akkermansia和3-IAA,证实了外源性补充3-IAA可能有助于减缓HM的进展,点明了肠道-眼轴的存在。这些结论不仅增进了我们对HM与肠道菌群之间关系的理解,而且为开发新的治疗HM的方法提供了科学依据。
此外,也给予了我们一些新思路,人体是一个整体,所有器官都具有相关联系,肠道菌群可能可以影响所有器官,同样的思路,换个研究对象,可能就是新的研究内容。
参考文献:
[1] Li, Hao et al. “Gut microbiota-derived indole-3-acetic acid suppresses high myopia progression by promoting type I collagen synthesis.” Cell discovery vol. 10,1 89. 27 Aug. 2024, doi:10.1038/s41421-024-00709-5


